Seleni (Se), un element químic del grup oxigen (Grup 16 [VIa] de la taula periòdica), estretament relacionat amb propietats físiques i químiques amb els elements sofre i teluri. El seleni és rar, compost aproximadament 90 parts per mil milions de l'escorça de la Terra. De vegades es troba sense combinar, acompanyant sofre autòcton, però es troba més sovint en combinació amb metalls pesants (coure, mercuri, plom o plata) en alguns minerals. La principal font comercial de seleni és un subproducte de refinació del coure; els seus principals usos són en la fabricació d’equips electrònics, en pigments i en la fabricació de vidre. El seleni és un metaloide (un element intermedi en propietats entre els metalls i els no metalls). La forma grisa i metàl·lica de l’element és la més estable en condicions ordinàries; aquesta forma té la propietat insòlita d’augmentar molt la conductivitat elèctrica quan s’exposa a la llum. Els compostos de seleni són tòxics per als animals; les plantes cultivades en sòls selenífers poden concentrar l’element i convertir-se en verinoses.
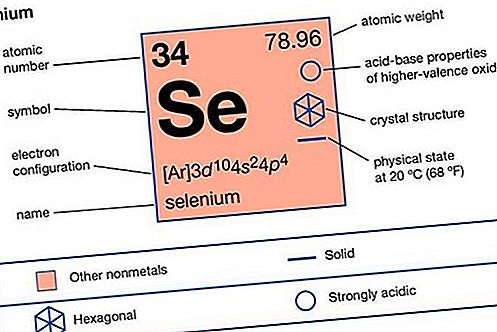

element del grup d’oxigen: Aparició i usos naturals
L'element de seleni (símbol Se) és molt més rar que l'oxigen o el sofre, i inclou aproximadament 90 parts per mil milions de l'escorça de
.Propietats dels elements
| nombre atòmic | 34 |
|---|---|
| pes atòmic | 78,96 |
| masses d’isòtops estables | 74, 76, 77, 78, 80, 82 |
| punt de fusió | |
| amorfa | 50 ° C (122 ° F) |
| gris | 217 ° C (423 ° F) |
| punt d'ebullició | 685 ° C (1.265 ° F) |
| densitat | |
| amorfa | 4,28 grams / cm 3 |
| gris | 4,79 grams / cm 3 |
| estats d’oxidació | −2, +4, +6 |
| configuració d’electrons | 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 4 |
Història
El químic suec Jöns Jacob Berzelius el 1817 va assenyalar una substància vermella resultant de minerals sulfurs de les mines de Falun, Suècia. Quan es va investigar aquest material vermell l'any següent, va resultar ser un element i va rebre el nom de la Lluna o la deessa Selene de la Lluna. Berzelius va descobrir un mineral de contingut inusualment alt de seleni només uns dies abans de fer el seu informe a les societats científiques del món sobre seleni. El seu sentit de l'humor es palesa en el nom que va donar el mineral, eucairite, que significa "just a temps".
Aparició i usos
La proporció de seleni a l'escorça terrestre és d'aproximadament 10 a 5 a 10-6 per cent. S'ha obtingut principalment a partir dels llims d'ànodes (dipòsits i materials residuals de l'ànode) en el refinament electrolític del coure i el níquel. Altres fonts són les polvores de combustió de la producció de coure i plom i els gasos formats en els rostits de pirites. El seleni acompanya el coure en l’afinació d’aquest metall: al voltant del 40 per cent del seleni present en el mineral original es pot concentrar en el coure dipositat en processos electrolítics. Es poden obtenir uns 1,5 quilograms de seleni a partir d’una tona de coure fosa.
Quan s’incorpora en petites quantitats al vidre, el seleni serveix de descoloritzador; en quantitats més grans, aporta als vidres un color vermell clar que és útil en els llums de senyal. L'element també s'utilitza per fabricar esmalts vermells per a ceràmica i articles d'acer, així com per a la vulcanització del cautxú per augmentar la resistència a l'abrasió.
Els esforços de perfeccionament del seleni són els més importants a Alemanya, Japó, Bèlgica i Rússia.
Allotropia
L’alotropia del seleni no és tan extensa com la del sofre i els al·lotròpics no s’han estudiat tan a fons. Només dues varietats cristal·lines de seleni estan compostes per molècules de Se 8 cícliques: designades α i β, totes dues existeixen com a cristalls monoclinics vermells. Un al·lotrop gris que té propietats metàl·liques es forma mantenint qualsevol de les altres formes a 200-220 ° C i és el més estable en condicions ordinàries.
Una forma amorfa (no cristal·lina), vermella i en pols de seleni, resulta quan una solució d’àcid seleniós o una de les seves sals és tractada amb diòxid de sofre. Si les solucions són molt diluïdes, les partícules extremadament fines d’aquesta varietat produeixen una suspensió coloidal vermella transparent. El vidre vermell clar resulta d’un procés similar que es produeix quan el vidre fos que conté selenites es tracta amb carboni. Una varietat de seleni verdós, gairebé negre, es forma pel refredament ràpid d’altres modificacions a temperatures superiors als 200 ° C. La conversió d'aquesta forma vitriosa a allotropes vermells i cristal·lins es produeix en escalfar-la per sobre de 90 ° C o en mantenir-la en contacte amb dissolvents orgànics, com cloroform, etanol o benzè.
Preparació
El seleni pur s’obté a partir dels llims i fangs formats per produir àcid sulfúric. El seleni vermell impur es dissol en àcid sulfúric en presència d’un agent oxidant, com el nitrat de potassi o certs compostos de manganès. Tant l'àcid seleniós, H 2 SeO 3, com l'àcid selènic, H 2 SeO 4, es formen i es poden filtrar a partir de materials insolubles residuals. Altres mètodes utilitzen l’oxidació per aire (torrefacció) i escalfament amb carbonat de sodi per donar selenita de sodi soluble, Na 2 SeO 3 · 5H 2 O i selenat de sodi, Na 2 SeO 4. També es pot emprar clor: la seva acció sobre selenurs metàl·lics produeix compostos volàtils, inclòs diclorur de seleni, SeCl 2; tetraclorur de seleni, SeCl 4; diclorur de diseleni, Se 2 Cl 2; i oxiclorur de seleni, SeOCl 2. En un procés, aquests compostos de seleni es converteixen per aigua en àcid seleniós. El seleni finalment es recupera tractant l’àcid seleniós amb diòxid de sofre.
El seleni és un component comú dels minerals valorats pel seu contingut en plata o coure; es concentra en els llims dipositats durant la purificació electrolítica dels metalls. S’han desenvolupat mètodes per separar el seleni d’aquests llims, que també contenen una mica de plata i coure. La fusió de llims forma selenur de plata, Ag 2 Se, i selenur de coure (I), Cu 2 Se. El tractament d’aquests selenids amb àcid hipoclorós, HOCl, proporciona selenites i selenites solubles, que es poden reduir amb diòxid de sofre. La purificació final del seleni s’aconsegueix mitjançant una destil·lació repetida.
Propietats físico-elèctriques
La propietat física més destacada del seleni cristal·lí és la seva fotoconductivitat: a la il·luminació, la conductivitat elèctrica augmenta més de 1.000 vegades. Aquest fenomen resulta de la promoció o excitació d’electrons relativament fluïts per la llum a estats d’energia més elevats (anomenats nivells de conducció), permetent la migració d’electrons i, per tant, la conductivitat elèctrica. En canvi, els electrons dels metalls típics ja es troben en nivells de conducció o bandes, capaços de fluir sota la influència d’una força electromotriu.
La resistivitat elèctrica del seleni varia entre un rang enorme, depenent de variables com la naturalesa de l’al·lotrop, les impureses, el mètode d’afinació, la temperatura i la pressió. La majoria de metalls són insolubles en seleni i les impureses no metàl·liques augmenten la resistivitat.
La il·luminació de seleni cristal·lí durant 0,001 segons augmenta la seva conductivitat en un factor de 10 a 15 vegades. La llum vermella és més eficaç que la llum de longitud d’ona més curta.
Són avantatges aquestes propietats fotoelèctriques i de fotosensibilitat del seleni en la construcció d'una varietat de dispositius que poden traduir variacions de la intensitat de la llum en corrent elèctric i, per tant, a efectes visuals, magnètics o mecànics. Els dispositius d’alarma, dispositius d’obertura i tancament mecànics, sistemes de seguretat, televisió, pel·lícules de so i xerografia depenen de la propietat semiconductora i la fotosensibilitat del seleni. Des de fa anys, la rectificació del corrent elèctric alternatiu (conversió en corrent directe) es realitza mitjançant dispositius controlats per seleni. Moltes aplicacions fotocèl·lules que utilitzen seleni han estat substituïdes per altres dispositius que utilitzen materials més sensibles, més fàcilment disponibles i més fàcils de fabricar que el seleni.













