Àcid nítric, (HNO 3), líquid incolor, fumegant i altament corrosiu (punt de congelació −42 ° C [−44 ° F], punt d'ebullició 83 ° C [181 ° F]) que és un reactiu de laboratori comú i important química industrial per a la fabricació d’adobs i explosius. És tòxic i pot provocar cremades greus.
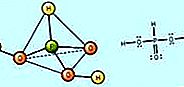
oxiàcid: Sales nítriques i nitrats
L’àcid nítric, HNO3, era conegut pels alquimistes del segle VIII com a “aqua fortis” (aigua forta). Es forma
Els alquimistes primerencs coneixien la preparació i l’ús d’àcid nítric. Un procés de laboratori comú utilitzat durant molts anys, atribuït a un químic alemany, Johann Rudolf Glauber (1648), consistia a escalfar nitrat de potassi amb àcid sulfúric concentrat. El 1776, Antoine-Laurent Lavoisier va mostrar que contenia oxigen i, el 1816, Joseph-Louis Gay-Lussac i Claude-Louis Berthollet van establir la seva composició química.
El principal mètode de fabricació d’àcid nítric és l’oxidació catalítica de l’amoníac. En el mètode desenvolupat pel químic alemany Wilhelm Ostwald el 1901, el gas d’amoníac s’oxida successivament a òxid nítric i diòxid de nitrogen per aire o oxigen en presència d’un catalitzador de gasa de platí. El diòxid de nitrogen s’absorbeix a l’aigua per formar àcid nítric. La solució àcid a l'aigua resultant (al voltant d'un 50-70 per cent en pes àcid) es pot deshidratar per destil·lació amb àcid sulfúric.
L’àcid nítric es descompon en aigua, diòxid de nitrogen i oxigen, formant una solució de color groc marró. És un àcid fort, completament ionitzat en ions hidroni (H 3 O +) i nitrats (NO 3 -) en solució aquosa i un agent oxidant potent (que actua com a acceptor d’electrons en reaccions de reducció de l’oxidació). Entre les moltes reaccions importants de l’àcid nítric destaquen: la neutralització amb l’amoníac per formar nitrat d’amoni, un component principal dels fertilitzants; nitració de glicerol i toluè, que formen els explosius nitroglicerina i trinitrotoluè (TNT), respectivament; preparació de nitrocel·lulosa; i oxidació de metalls als òxids o nitrats corresponents.













