El fòsfor (P), element químic no metàl·lic de la família de nitrogen (Grup 15 [Va] de la taula periòdica) que a temperatura ambient és un sòlid cerós incolor, semitransparent, suau i cerós que brilla a les fosques.
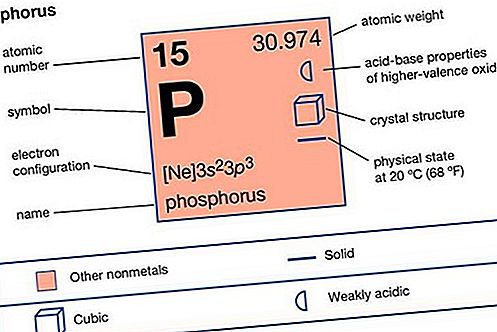
Propietats dels elements
| nombre atòmic | 15 |
|---|---|
| pes atòmic | 30.9738 |
| punt de fusió (blanc) | 44,1 ° C (111,4 ° F) |
| punt d'ebullició (blanc) | 280 ° C (536 ° F) |
| densitat (blanc) | 1,82 gram / cm 3 a 20 ° C (68 ° F) |
| estats d’oxidació | −3, +3, +5 |
| configuració d’electrons | 1s 2 2s 2 2p 6 3s 2 3p 3 |
Història

Els alquimistes àrabs del segle XII poden tenir un fòsfor elemental aïllat per accident, però els registres no són clars. Sembla que el fòsfor fou descobert el 1669 per Hennig Brand, un comerciant alemany l’afició del qual era l’alquímia. La marca va permetre que quedessin 50 galledes d’orina fins que van posar els cucs i els “cucs”. A continuació, va bullir l’orina fins a una pasta i la va escalfar amb sorra, destil·lant el fòsfor elemental de la barreja. Brand va informar del seu descobriment en una carta a Gottfried Wilhelm Leibniz, i, després, les demostracions d’aquest element i la seva capacitat de brillar a les fosques o “fosforescència” van excitar l’interès públic. El fòsfor, però, va romandre com a curiositat química fins aproximadament un segle després, quan va resultar ser un component dels ossos. La digestió d’ossos amb àcid nítric o sulfúric va formar àcid fosfòric, a partir del qual es podia destilar el fòsfor escalfant-se amb carbó vegetal. A finals del 1800, James Burgess Readman, d'Edimburg, va desenvolupar un mètode de forn elèctric per produir l'element a partir de roca fosfat, que és essencialment el mètode emprat en l'actualitat.
Ocupació i distribució
El fòsfor és un element molt distribuït, el 12è més abundant a la crosta d'Earth, al qual aporta aproximadament un 0,10 per cent de pes. La seva abundància còsmica és d'aproximadament un àtom per cada 100 àtoms de silici, l'estàndard. La seva alta reactivitat química assegura que no es produeix en estat lliure (excepte en alguns meteorits). El fòsfor sempre es produeix com el ió fosfat. Les formes combinades principals a la natura són les sals fosfats. S'han trobat al voltant de 550 minerals diferents que contenen fòsfor, però, entre ells, la principal font de fòsfor és la sèrie d'apatita en la qual existeixen ions de calci juntament amb ions fosfat i quantitats variables de ions fluor, clorur o hidròxid, segons la fórmula [Ca 10 (PO 4) 6 (F, Cl, o OH) 2]. Altres minerals importants que contenen fòsfor són wavellita i vivianita. Comunament, àtoms metàl·lics com magnesi, manganès, estronci i plom substitut per al calci al mineral, i silicats, sulfats, vanadats i anions similars substitueixen els ions fosfat. Es troben jaciments sedimentaris molt grans de fluoroapatita a moltes parts de la Terra. El fosfat d’os i esmalt dental és hidroxiapatita. (El principi de disminuir la càries dental per fluoruració depèn de la conversió de la hidroxiapatita a la fluoroapatita més dura, més resistent a la càries).
La principal font comercial és el fosfat, o roca fosfat, una forma massiva impura d’apatita portant carbonat. Les estimacions de la roca fosfat total a l'escorça terrestre medien unes 65.000.000.000 tones, de les quals el Marroc i el Sàhara Occidental contenen aproximadament el 80 per cent. Aquesta estimació només inclou el mineral prou ric en fosfat per convertir-lo en productes útils segons els mètodes actuals. Existeixen nombroses quantitats de material amb contingut inferior en fòsfor.

L’únic isòtop del fòsfor que es produeix naturalment és el de la massa 31. Els altres isòtops de la massa 24 a la massa 46 s’han sintetitzat per reaccions nuclears adequades. Totes elles són radioactives amb semivides relativament curtes. L’isòtop de la massa 32 té una semivida de 14.268 dies i s’ha demostrat extremadament útil en estudis de traçadors que comporten l’absorció i el moviment del fòsfor en els éssers vius.